Behandling af primær osteoporose i almen praksis
Artikel fra Rationel Farmakoterapi 2, 2019
Månedsbladet opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
Kamilla Grønborg Laut1, Johan Reventlow2, Lars Rejnmark3
Mere end 172.000 personer, svarende til knap 3% af den danske befolkning, er diagnosticeret med osteoporose (knogleskørhed), og ca. 90.000 personer får receptpligtig medicin herfor [1, 2]. Antallet af mennesker, der lever med udiagnosticeret osteoporose, er formentlig 2-3 gange højere [1]. Risikoen for at udvikle osteoporose stiger med alderen og er hyppigere blandt kvinder end blandt mænd.
Osteoporose er karakteriseret ved forandringer i knoglevævet, som gør knoglestrukturen mere porøs, hvorved risikoen for fraktur øges. De hyppigste frakturer ved osteoporose er i underarm (Colles-fraktur), ryghvirvler og hofte, og er lavenergifrakturer, dvs. frakturer, der opstår i forbindelse med almindelig daglig belastning eller fald fra samme niveau [3].
Hovedfokus for denne artikel er farmakologisk behandling af primær osteoporose, dvs. osteoporose, hvor en enkelt årsag til sygdommen ikke kan identificeres. Hos kvinder kan ca. en tredjedel og hos mænd ca. to tredjedele af tilfældene af osteoporose imidlertid kobles til en underliggende sygdom eller risikofaktor (fx glukokortikoidbehandling) og betegnes da sekundær osteoporose [4]. Overordnet set er der sparsom evidens for behandling af osteoporose blandt mænd, men den kliniske erfaring er betydelig [5]. Anbefalingerne i denne artikel omfatter således også mænd > 60 år med osteoporose.
|
Boks 1.Hovedbudskaber |
|
Opsporing og diagnostik
Diagnosen osteoporose kan stilles på baggrund af en dual X-ray absorptiometry (DXA)-skanning med måling af knoglemineraltætheden (BMD) i hofteregionen og i lumbalcolumna. En T-score, der ligger mere end -2,5 standarddeviationer under, hvad der er normalt for raske, yngre individer af samme køn, er diagnostisk for osteoporose. T-score mellem -1 og -2,5 klassificeres som osteopeni. Ved osteoporose eller lavenergibrud suppleres med blodprøver mhp. at udelukke sekundær osteoporose (fx kronisk nyreinsufficiens, calcium- eller D-vitaminmangel) og udelukke differentialdiagnoser (fx knoglemetastaser).
En række risikofaktorer disponerer til udvikling af osteoporose og kan give anledning til en risikovurdering og evt. DXA-skanning (Boks 2). Desuden bør en lavenergifraktur give mistanke om osteoporose og bør normalt føre til udredning [3, 4, 6]. Lavenergifrakturer i ryg og/eller hofte er diagnostisk for osteoporose. Hos disse patienter er DXA-skanning ikke absolut indiceret, men foretages mhp. vurdering af sværhedsgrad og monitorering af behandlingseffekt. En lateral røntgenoptagelse af columna kan endvidere være indiceret ved mistanke om sammenfald af ryghvirvler.
|
Boks 2. Indikationer for DXA-skanning |
|
DXA-skanning overvejes ved mindst én af følgende risikofaktorer [2-6].
Stærke risikofaktorer
Kliniske tegn på osteoporose
Sygdom, som disponerer til osteoporose(fx KOL, reumatoid artritis, kronisk nyreinsufficiens, malabsorption m.fl.)
Øvrige risikofaktorer, der kan øge risikoen for osteoporose og/eller fraktur omfatter: tobaksrygning, stort alkoholforbrug, behandling med aromatasehæmmer eller antiandrogene stoffer, immobilisering m.fl. |
Farmakologisk behandling
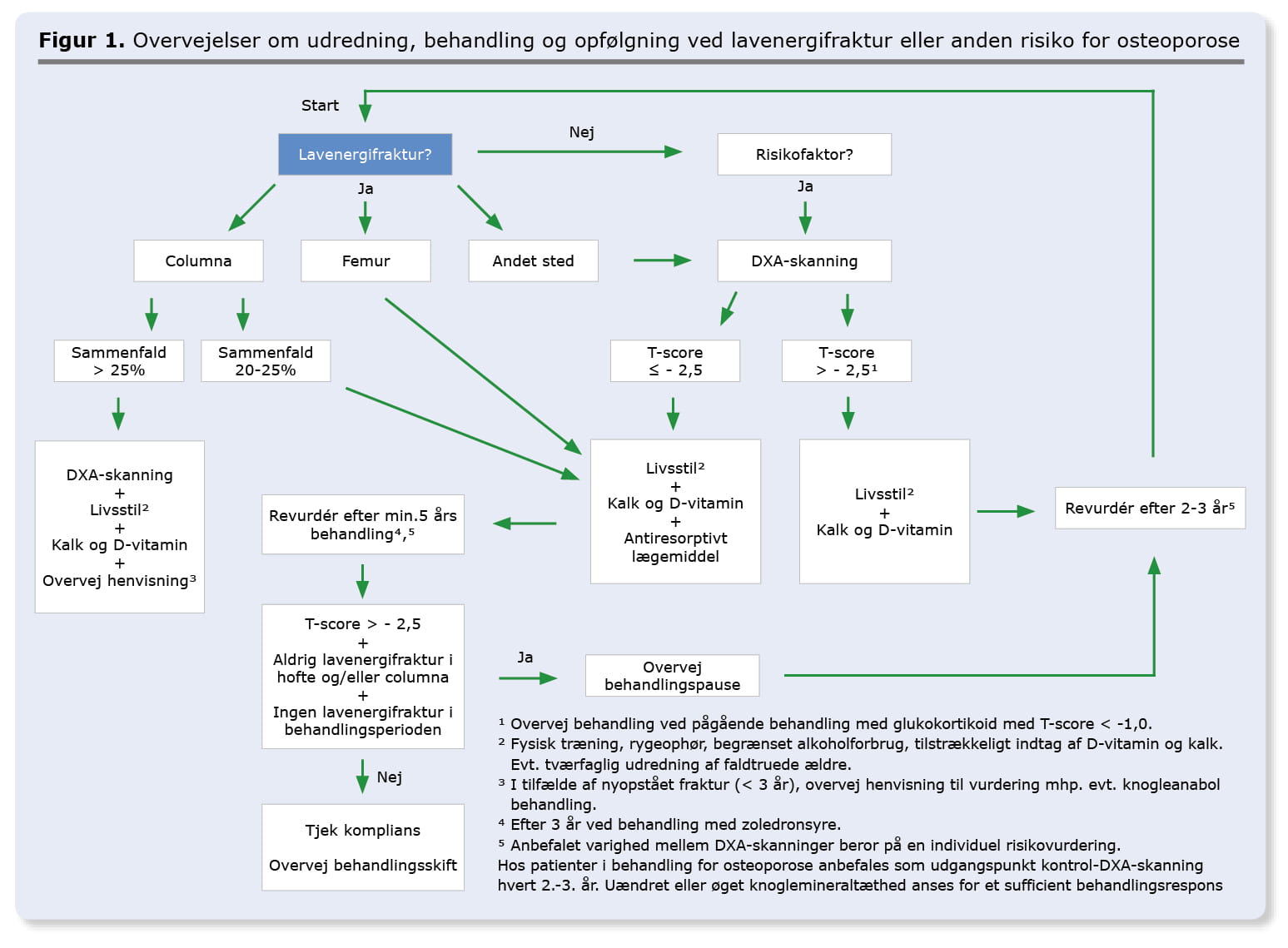
Formålet med farmakologisk behandling af osteoporose er at reducere risikoen for fraktur. Behandling er indiceret ved lavenergifraktur i ryg eller hofte, T-score < -4,0 eller T-score < -2,5 med samtidig tilstedeværelse af risikofaktorer (Figur 1, Boks 2). Endvidere kan der, pga. risiko for udvikling af sekundær osteoporose, være indikation for at behandle osteopene patienter, som er i behandling med glukokortikoid [4]. Der er klausuleret tilskud til alendronat til patienter med lavenergifraktur i hofte. Derudover kan der søges enkelttilskud jf. Lægemiddelstyrelsens vejledning [7].
Lægemidler mod osteoporose inddeles i antiresorptive (knoglebevarende) og anabole (knogleopbyggende) præparater. Behandling med antiresorptive præparater kan som udgangspunkt iværksættes og varetages i almen praksis under hensyntagen til patientens ønsker, samlede risikoprofil og forventede restlevetid. Førstevalg er de perorale (p.o.) bisfosfonater alendronat eller risedronat. Hvis disse ikke tåles, hvis der er problemer med komplians, ved kontraindikationer eller ved behandlingssvigt, kan anden behandling overvejes. Andetvalg er fortrinsvis zoledronsyre intravenøst (i.v.) hver 12. måned eller denosumab subkutant (s.c.) hver 6. måned.
Kalcium og d-vitamin
Forud for iværksættelse af farmakologisk behandling anbefales det at sikre, at patienten har en sufficient D-vitaminniveau (plasma 25-hydroxyvitamin D > 50 nmol/l). Under pågående behandling anbefales kosttilskud med kalcium (800-1.000 mg/dag) og D-vitamin (typisk 20-40 mcg/800-1.600 IE dagligt) mhp. at sikre optimale forhold for knoglemineralisering og for at mindske risikoen for hypokalcæmi. Dosis kan evt. reduceres ved et habituelt højt indtag gennem kosten.
Bisfosfonater
Bisfosfonaterne hæmmer osteoklastaktiviteten og har en antiresorptiv effekt. Bisfosfonater er indicerede til kvinder og mænd med osteoporose [5]. Alendronat og risedronat betragtes som ligeværdige i forhold til at beskytte mod nonvertebrale, vertebrale frakturer og hoftefrakturer. Derimod er der for ibandronat alene evidens for, at det reducerer risikoen for vertebrale frakturer, hvorfor dette præparat ikke er førstevalg [8].
Bivirkningsprofilen for bisfosfonater er overordnet benign. Der er klinisk erfaring for, at øvre gastrointestinale (GI)-gener er en hyppigt forekommende bivirkning til bisfosfonater, men en overhyppighed af GI-gener, herunder mavesår, gastritis m.fl., blev ikke genfundet i en evidensgennemgang [8, 9]. Sjældne, men alvorlige, bivirkninger til bisfosfonatbehandling er kæbeosteonekrose og atypiske hoftefrakturer. Formodede risikofaktorer for kæbeosteonekrose er bl.a. kumulativ dosis, cancer, glukokortikoider, kemoterapi samt dårlig tandstatus [10]. En forebyggende tandlægebehandling kan overvejes før behandling hos patienter med dårlig tandstatus mhp. forebyggelse af kæbeosteonekrose [11-13]. Atypiske hoftefrakturer ses primært hos patienter i langtidsbehandling [14]. Uforklarede smerter i lyske eller lårben hos en osteoporosepatient bør give mistanke om atypisk hoftefraktur, selv efter et minimalt traume. Behandling med bisfosfonater er kontraindiceret ved betydelig nedsat nyrefunktion og hypokalcæmi, samt, for p.o.præparater, ved tilstande, der kan forlænge passagetiden gennem spiserøret [11].
Biotilgængeligheden ved p.o.bis- fosfonat er lav, hvorfor regimet for indtag er strikt. For at opnå tilstrækkelig absorption skal bisfosfonatet indtages med vand om morgenen i siddende eller oprejst stilling og efterfølges af mindst 30 minutters faste (på nær postevand). Patienten frarådes at ligge ned i mindst 30 minutter efter indtag af tabletten for at mindske risikoen for øsofageale bivirkninger.
Ved problemer med komplians til p.o.bisfosfonat eller ved behandlingssvigt kan det overvejes at henvise patienten til behandling med i.v.zole- dronsyre hver 12. måned. Den frakturreducerende effekt af zoledronsyre er veldokumenteret, og præparatet har en bivirkningsprofil, der ligner de andre bisfosfonaters [9, 15]. Dog er hyppigheden af alvorlige bivirkninger, som atypisk hoftefraktur og kæbe-osteonekrose, højere [16].
RANK-ligand-antistof
Denosumab er et monoklonalt antistof, som, ved at binde til RANKL, hæmmer osteoklastaktiviteten. Denosumab kan gives til kvinder og mænd og gives s.c. hver sjette måned. Lægemidlet har en dokumenteret beskyttende effekt mod vertebrale og nonvertebrale frakturer samt hoftefrakturer. Bivirkninger af denosumab omfatter øvre GI-bivirkninger, en øget forekomst af infektioner (cellulitis, øvre luftvejsinfektioner og urinvejsinfektioner) samt muskuloskeletale bivirkninger. Alvorlige bivirkninger omfatter en øget risiko for svære infektioner (dvs. som kræver i.v.behandling, indlæggelse eller kan være dødelig). Det estimeres, at der vil opstå en alvorlig infektion for hver 120 personer, der behandles med denosumab i tre år [8]. Ligesom ved bisfosfonater, og med samme risikofaktorer, er der observeret tilfælde af kæbeosteonekrose og atypiske hoftefrakturer under behandling med denosumab. Endelig har der været indberetninger om en øget hyppighed af vertebrale frakturer inden for det første år efter ophør med denosumab. Evidensen for dette er ikke entydig, men usikkerheden om en risiko for ophobning af vertebrale frakturer har givet anledning til, at man anbefaler at overveje skift til et andet antiresorptivt præparat (fx bisfosfonat) seks måneder efter sidste administration af denosumab [3, 6].
Behandling med denosumab er kontraindiceret ved hypokalcæmi, og patientens kalciumniveau bør altid måles før indgift. Behandlingen er endvidere kontraindiceret ved ikke-ophelede, åbne bløddelslæsioner i munden, pga. risikoen for kæbeosteonekrose.
Selektive østrogenreceptormodulatorer
Raloxifen har en antagonistisk effekt på fx mamma- og endometrievæv, men en agonistisk effekt på østrogenreceptorer i knoglerne, hvorved nedbrydningen af knoglevævet hæmmes. Raloxifen kan kun anvendes af kvinder og efter menopausen. Præparatet gives p.o. dagligt og kan tages på ethvert tidspunkt af dagen, uden hensyntagen til måltider. Raloxifen har en dokumenteret frakturreducerende effekt på vertebrale frakturer. Præparatet rekommanderes dog kun i særlige tilfælde, pga. en øget risiko for tromboemboliske bivirkninger (venetrombose, lungeemboli) og apopleksi og pga. begrænset evidens vedr. effekt på nonvertebrale frakturer og hoftefrakturer [8].
Anabole præparater
Behandling med anabole lægemidler (teriparatid) er indiceret hos postmenopausale kvinder og mænd over 40 år, som inden for de sidste tre år har pådraget sig en lavenergifraktur i ryggen (> 25% sammenfald), og som har en T-score i ryg eller hofte < -3,0, eller som har to eller flere lavenergifrakturer i ryggen (> 25% sammenfald) [3, 6]. Behandlingen bør iværksættes og varetages i samarbejde med en speciallæge i endokrinologi, reumatologi, geriatri og/eller intern medicin, som har erfaring med denne type behandling. Behandling med et anabolt lægemiddel gives typisk i to år, hvorefter der skiftes til antiresorptiv behandling [3, 4, 6, 11].
Opfølgning og behandlingsvarighed
Der foreligger ikke evidens for optimal behandlingsvarighed eller kontrol af behandlingsrespons ved osteoporose [11, 17]. Kontrol-DXA-skanning anvendes typisk til monitorering af behandlingsrespons, og en stigende eller stagnerende BMD tolkes som et positivt behandlingsrespons. Et fald i BMD, der overstiger de ca. 3-5%, der kan tilskrives måleusikkerhed, betragtes som signifikant [3, 4]. Sammenhængen mellem BMD og frakturrisiko er imidlertid ikke veletableret.
Pausering af alendronat kan forsøges efter fem år, og af zoledronsyre efter tre år, hvis patienten aldrig har haft en fraktur i ryg eller hofte, ikke har haft en lavenergifraktur i behandlingsperioden og T-score > -2,5 [3, 4, 6]. Ved knoglemineraltab eller lavenergifraktur under pågående behandling bør behandlingen derimod ikke pauseres. I stedet forsøges understøttelse af komplians, eller behandlingsskift kan overvejes (Figur 1). Efter pausering vil bisfosfonat, som er akkumuleret i knoglevævet, langsomt frigives, hvilket på sigt medfører et fald i BMD (faldende T-score). Det er ikke klart, hvordan patienter bør observeres efter ophør med behandlingen, eller hvornår denne eventuelt bør genoptages [3, 17]. Som udgangspunkt anbefales kontrol-DXA-skanning 1-2 år efter pausering og derefter hvert andet år. Behandlingen overvejes genoptaget ved T-score < -2,5. Skanning på samme skanner foretrækkes mhp. at mindske måleusikkerhed mellem skannere.
Behandling med raloxifen eller denosumab bør ikke pauseres uden stillingtagen til evt. behandlingsalternativ (fx bisfosfonat), idet disse lægemidler, i modsætning til bisfosfonat, ikke akkumuleres i knoglevævet under pågående behandling [18].
Nonfarmakologiske tiltag
Nonfarmakologisk frakturprofylakse omfatter knoglevenlig livsstil, herunder en kost, der indeholder tilstrækkeligt kalcium og D-vitamin, fysisk aktivitet, rygeophør samt et begrænset alkoholindtag. Derudover kan der være behov for smertebehandling, indsatser vedr. sygdomsmestring, tværfaglig udredning af faldtruede ældre mv. [1, 19].
Osteoporosepatienter anbefales en kombination af aerob træning og styrketræning mhp. at styrke knoglemineraltætheden og forebygge fald [20]. Borgere med osteoporose kan henvises til tilbud til borgere med udvalgte kroniske sygdomme, som tilbydes i de fleste kommuner i landet [21]. Nogle kommuner og regioner har endvidere etableret specifikke tilbud (osteoporoseskoler) til osteoporosepatienter hhv. uden og med fraktur. Der er endvidere mulighed for at tilrettelægge rehabiliteringsindsatser gennem kommunernes opsøgende og forebyggende hjemmebesøg (som tilbydes alle ældre ≥ 75 år, eller fra 65-årsalderen, hvis der er særlige behov). Endelig er der indikation for en tværfaglig udredning af faldtruede ældre, ligesom medicin, der kan forårsage svimmelhed, bør gennemgås og evt. saneres [19, 22].
Henvisning
Følgende patienter bør normalt tilbydes henvisning til speciallæge i endokrinologi, reumatologi, geriatri og/eller intern medicin, mhp. behandling samt evt. yderligere udredning:
- Patienter med ≥ 2 lavenergifrakturer i ryggen mhp. evt. knogleanabol behandling
- Patienter med behandlingssvigt (≥ 2 lavenergifrakturer eller > 3-5% reduktion af BMD under pågående behandling)
- Præmenopausale kvinder og mænd < 60 år, uden oplagt årsag til osteoporose.
Se www.irf.dk for tabel 2 for Number needed to treat (NNT) for udvalgte lægemidler mod osteoporose.
|
Tabel 1.Oversigt over rekommanderede præparater til behandling af osteoporose i almen praksis |
|||||
|
Præparat |
Dosis |
Bivirkninger (udvalgte) |
Interaktioner (udvalgte) |
Kontra-indikationer |
Pris for 1 års behandlingb |
|
Alendronata |
70 mg p.o. ugentligt |
|
|
|
153 kr. |
|
Risedronat |
35 mg p.o. ugentligt |
438 kr. |
|||
|
Denosumab |
60 mgs.c. hver6 måned |
|
|
|
4.690 kr. |
|
a) Alendronat er kun godkendt til mænd i en dosis på 10 mg dagligt, til trods for betydelig klinisk erfaring med doseringen 70 mg ugentligt. b) Pris for 1 års behandling med anbefalet dosis. www.medicinpriser.dk (9. jan 2019). |
|||||
Habilitetserklæringer
1) Kamilla Grønborg Laut, Indsatser for Rationel Farmakoterapi, Center for Evidens, Uddannelse og Beredskab, Sundhedsstyrelsen
2) Johan Reventlow, Lægerne Reventlow, Wolfhagen og Bendtsen, Slagelse
3) Lars Rejnmark, Medicinsk Endokrinologisk Afdeling, Aarhus Universitetshospital
Pdf-version
Hele månedsbladet kan læses i pdf-version
Referencer
- Sundhedsstyrelsen. En afdækning af den samlede indsats mod osteoporose. Sundhedsstyrelsen, 2018.
- Sundhedsdatastyrelsen. Prævalens, incidens og behandling i sundhedsvæsenet for borgere med osteoporose. Bilagspublikation – en afdækning i tal af den samlede indsats mod osteoporose. Sundhedsdatastyrelsen, 2018.
- Dansk Endokrinologisk Selskab. National Behandlingsvejledning (NBV): Behandlingsvejledning i osteoporose hos kvinder, opdateret 2016. http://www.endocrinology.dk/index.php/3-calcium-og-knoglemetaboliske-sygdomme/3-osteoporose (4. dec 2018).
- Dansk Knoglemedicinsk Selskab. Vejledning til udredning og behandling af osteoporose, 2009 (opdateret 2012). http://wp.dkms.dk/?page_id=1049 (4. dec 2018).
- Sundhedsdatastyrelsen. Medstat.dk. http://medstat.dk/(4. dec 2018).
- Dansk Endokrinologisk Selskab. National Behandlingsvejledning (NBV): Behandling af mandlig osteoporose. http://www.endocrinology.dk/index.php/3-calcium-og-knoglemetaboliske-sygdomme/nbv-endokrinologi-behandling-af-mandlig-osteoporose-sekundaer-osteoporose-mandlig-hypogonadisme-d-vitamin (4. dec 2018).
- Lægemiddelstyrelsen. Vejledende kriterier for enkelttilskud, 2016. https://laegemiddelstyrelsen.dk/da/tilskud/individuelle-tilskud/enkelttilskud/vejledende-kriterier (13. dec 2018).
- Sundhedsstyrelsen. Den Nationale Rekommandationsliste: Farmakologisk behandling af primær osteoporose. Sundhedsstyrelsen, 2019.
- National Institute for Health and Care Excellence, NICE. Multiple technology appraisal: bisphosphonates for preventing osteoporotic fragility fractures (including a partial update of NICE technology appraisal guidance 160 and 161), 2017.
- European Medicines Agency. CHMP assessment report on bisphosphonates and osteonecrosis of the jaw. EMEA/CHMP/291125, 2009.
- Compston J, Cooper A, Cooper C et al. UK clinical guideline for the prevention and treatment of osteoporosis. Arch Osteoporos 2017;12:43.
- European Medicines Agency. Produktresume for Aclasta. Opdateret 2018. EMEA/H/C/000595 - T/0070.
- Lægemiddelstyrelsen. Produktresumé for Fosamax Ugetablet. D.Sp.Nr. 9162. Opdateret 2018.
- European Medicines Agency. Assessment report for bisphosphonates containing medicinal products. EMA/725125, 2011.
- Zhou J, Ma X, Wang T et al. Comparative efficacy of bisphosphonates in short-term fracture prevention for primary osteoporosis: a systematic review with network meta-analyses. Osteoporos Int 2016;27:3289-300.
- European Medicines Agency. PRAC recommends further measures to minimise risk of osteonecrosis of the jaw with bisphosphonate medicine. EMA/169618, 2015.
- Black DM, Bauer DC, Schwartz AV et al. Continuing bisphosphonate treatment for osteoporosis – for whom and for how long? NEJM 2012;366:2051-3.
- Tsourdi E, Langdahl B, Cohen-Solal M et al. Discontinuation of Denosumab therapy for osteoporosis: a systematic review and position statement by ECTS. Bone 2017;105:11-7.
- Sundhedsstyrelsen. Nationale kliniske retningslinjer for forebyggelse af fald. Version 1.1. Sundhedsstyrelsen, 2018.
- Sundhedsstyrelsen. Fysisk træning som behandling – 31 lidelser og risikotilstande. Version 1.2. Sundhedsstyrelsen, 2018.
- Sundhedsstyrelsen. Anbefalinger for forebyggelsestilbud til borgere med kronisk sygdom. Sundhedsstyrelsen, 2016.
- Sund By Netværket. 8 anbefalinger til forebyggelse af ældres faldulykker – den gode kommunale model. 2. reviderede udgave. Sund By Netværket, 2016.