Information til læger om COVID-19 vacciner, der ikke indgår i det generelle vaccinationsprogram mod COVID-19
Artikel fra Rationel Farmakoterapi 2, 2021

Månedsbladet opdateres ikke efter udgivelsen. Indholdet afspejler den aktuelle evidens på udgivelsestidspunktet.
Maria Tølbøll Glavind1, Kamilla Grønborg Laut2, Marie Louise Schougaard Christiansen3
1) Sundhedsstyrelsen, Enhed for Beredskab og smitsomme sygdomme
2) Sundhedsstyrelsen, Enhed for Primære sundhedsvæsen
3) Sundhedsstyrelsen, Enhed for Evidensbaseret medicin
COVID-19 forårsages af ny coronavirus (SARS-CoV-2), der kan give alvorlige, indlæggelseskrævende sygdomsforløb og øget risiko for død. Danmark påbegyndte den 27. december 2020 det generelle vaccinationsprogram mod COVID-19. Det overordnede formål med det generelle vaccinationsprogram er at forebygge alvorlig sygdom og død [1]. Alle danskere over 16 år vil som led i det generelle vaccinationsprogram mod COVID-19 blive tilbudt gratis vaccination [2].
Alvorlige bivirkninger ved Vaxzevria® og COVID-19 Vaccine Janssen®
Det Europæiske Lægemiddelagentur (EMA) og de amerikanske lægemiddelmyndigheder har efter ibrugtagning af Vaxzevria® og COVID-19 Vaccine Janssen® konkluderet, at der er en sandsynlig sammenhæng mellem vaccinerne og sjældne tilfælde af Vaccine-induceret Immun Trombotisk Trombocytopeni (VITT) [3-5]. Det er også blevet diskuteret i videnskabelige publikationer [6, 7].
Sundhedsstyrelsen har vurderet, at den gavnlige effekt ved disse to vacciner i den aktuelle danske kontekst ikke opvejer den mulige risiko for VITT efter vaccination. Det generelle vaccinationsprogram fortsætter derfor aktuelt uden brug af Vaxzevria® og COVID-19 Vaccine Janssen® [8, 9], men disse vacciner gøres tilgængelige i en tilvalgsordning efter konkret lægelig ordination.
I det følgende gennemgås information til læger om de aktuelt EMA-godkendte COVID-19 vacciner, der ikke indgår i det generelle vaccinationsprogram mod COVID-19. I et elektronisk tillæg til denne artikel gennemgås vaccineteknologi, effekt og bivirkninger i detaljer.
Vaccineteknologi
Både COVID-19 Vaccine Janssen® og Vaxzevria® bruger en adenovirusvektor, hvis DNA er modificeret, så den ikke kan replikere sig selv, og så den koder for S-protein (spike glycoprotein) i SARS-CoV-2. Virusvektoren muliggør, at vaccinens DNA kan optages i kroppens celler og kode for dannelse af S-protein, som derefter indbygges i cellens overflade, hvor det præsenteres for kroppens immun-system, så der rejses et immunrespons.
Vaccination med COVID-19 Vaccine Janssen® består af én dosis mens et vaccinationsregime med Vaxzevria® består af to doser, givet med 4-12 ugers mellemrum. En nærmere beskrivelse af håndtering af vaccinerne, og kontraindikationer og forsigtighedsregler findes i produktresuméerne [10, 11].
Myndighedsbeslutninger ifm. sikkerhedssignaler ved Vaxzevria® og COVID-19 Vaccine Janssen®
25. marts 2021: Sundhedsstyrelsen forlænger pauseringen af Vaxzevria® yderligere tre uger
7. april 2021: EMA finder en sandsynlig sammenhæng mellem Vaxzevria® og VITT
9. april 2021: EMA indleder en sikkerhedssignalprocedure vedrørende COVID-19 Vaccine Janssen®
14. april 2021: Sundhedsstyrelsen fortsætter udrulningen af det generelle vaccinationsprogram i Danmark uden Vaxzevria®
20. april 2021: EMA finder en sandsynlig sammenhæng mellem COVID-19 Vaccine Janssen® og VITT
23. april 2021: De amerikanske lægemiddelmyndigheder finder en sandsynlig sammenhæng mellem COVID-19 Vaccine Janssen® og VITT
3. maj 2021: Sundhedsstyrelsen fortsætter det generelle vaccinationsprogram i Danmark uden COVID-19 Vaccine Janssen®
Effekt og sikkerhed ved COVID-19 Vaccine Janssen® og Vaxzevria® – godkendelsesgrundlaget
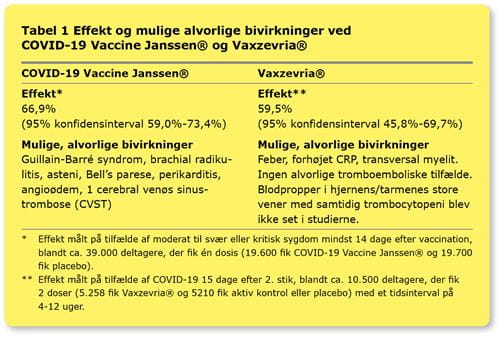
Godkendelsesgrundlaget for den betingede markedsføringstilladelse af COVID-19 Vaccine Janssen® og Vaxzevria® blev vurderet på baggrund af kliniske studier med deltagelse af personer fra 18 år og ældre. I Tabel 1 opsummeres effekten samt mulige, alvorlige bivirkninger observeret i de kliniske godkendelsesstudier. I det følgende gennemgås effekt og bivirkninger ved de to vacciner. For yderligere detaljer henvises til det elektroniske bilag.COVID-19 Vaccine Janssen®
Effekten af COVID-19 Vaccine Janssen® blev vurderet på baggrund af et igangværende klinisk studie med deltagelse af personer over 18 år. I den samlede effektanalyse indgik ca. 39.300 personer, hvoraf ca. 19.600 fik COVID-19 Vaccine Janssen® og ca. 19.700 fik placebo. Det primære effektmål var forebyggelse af moderat til svær eller kritisk COVID-19, bekræftet ved PCR-test, og med symptomdebut hhv. mindst 14 dage og 28 dage efter vaccination. Der var i alt 116 tilfælde af moderat til svær eller kritisk COVID-19 med debut mindst 14 dage efter vaccination blandt 19.630 personer, der fik COVID-19 Vaccine Janssen®, og 348 tilfælde blandt 19.691 personer, der fik placebo. Det svarer til, at COVID-19 Vaccine Janssen® havde en samlet effekt på 66,9% (95% konfidensinterval 59,0%-73,4%). Effekten var tilsvarende for moderat til svær eller kritisk COVID-19 med debut mindst 28 dage efter vaccination (66,9% (95% konfidensinterval 59,0%-73,4%)). Effekten alene målt på alvorlig COVID-19 var efter mindst 14 dage på 76,7% (95% konfidensinterval 54,6%-89,1%) og efter mindst 28 dage 85,4% (95% konfidensinterval 54,2%-96,9%).
De fleste formodede bivirkninger til COVID-19 Vaccine Janssen® (fx hovedpine, træthed, muskel- og ledsmerter og kvalme) var af mild til moderat intensitet, og symptomerne fortog sig oftest inden for 1-2 dage. Der blev set mulige, alvorlige bivirkninger blandt 0,4% af alle studiedeltagere. For 7 blev der vurderet, at der kunne være en sammenhæng med vaccinen (se Tabel 1) [11].
Vaxzevria®
Godkendelsesgrundlaget for den betingede markedsføringstilladelse af Vaxzevria® inkluderede data fra fire studier udført på personer fra 18 år. To indgik i opgørelsen af vaccinens effekt, og alle fire indgik i opgørelsen af bivirkninger. Den primære effektanalyse af Vaxzevria® blev opgjort på i alt ca. 10.500 studiedeltagere, der fik 2 doser med et tidsinterval på 4-12 uger. Heraf fik 5.258 personer Vaxzevria® og 5.210 personer aktiv kontrol eller placebo. Der var i alt 64 tilfælde af COVID-19 blandt 5.258 personer, der fik Vaxzevria®, og 154 tilfælde blandt 5.210 personer, der fik aktiv kontrol eller placebo. Det svarer til, at Vaxzevria® havde en samlet effekt på 59,5% (95% konfidensinterval 45,8%-69,7%). Den mediane opfølgningstid efter 2. dosis var 78 dage.
De fleste formodede bivirkninger til Vaxzevria® (fx hovedpine, træthed, muskel- og ledsmerter, kvalme og feber) var af mild til moderat intensitet, og symptomerne fortog sig oftest inden for få dage. Der blev set mulige, alvorlige bivirkninger blandt <1% af alle studiedeltagere. For 3 blev der vurderet, at der kunne være en sammenhæng med vaccinen (se Tabel 1) [10].
VITT-syndromet
Det kliniske billede ved VITT er karakteriseret ved intens, vedvarende hovedpine og/eller intense, abdominale smerter, og progressive eller atypiske trombose(r), særlig cerebral venøs sinustrombose (CVST), men også store tromboser i splanknikus-venerne og arterielle tromboser er beskrevet. Blødning kan ses i huden og andre steder, og i enkelte tilfælde er der set letale intrakranielle blødninger. Biokemisk ses altid udtalt trombocytopeni (<150 mia/L), betydelig forhøjet fibrin D-dimer, ofte et reduceret fibrinogen niveau samt påvisning af antistoffer mod Platelet Factor 4 (PF-4).
Sammenhæng mellem VITT og COVID-19 Vaccine Janssen® eller Vaxzevria®
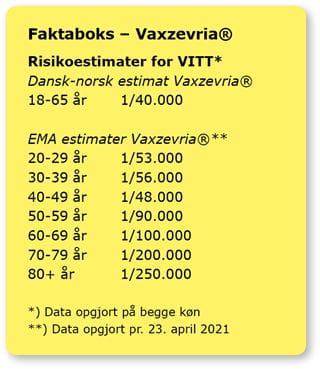
Der er fastlagt kausalitet mellem vaccination med COVID-19 Vaccine Janssen® eller Vaxzevria® og forekomst af VITT [3-7]. Et dansk-norsk registerstudie har undersøgt sammenhængen mellem vaccination med én dosis Vaxzevria® og cerebral venetrombose, der er en fremtrædende del af VITT-syndromet. Hyppigheden af cerebrale venetromboser blandt ca. 280.000 personer under 65 år (median-alder 44 år, 78% kvinder) vaccineret med Vaxzevria® var 2,5 tilfælde pr. 100.000 vaccinerede (95% konfidensinterval 0,9-5,2) i de første 2 til 4 uger efter vaccination. Det er en betydelig overhyppighed sammenlignet med baggrundsbefolkningen, hvor der i en tilsvarende kort tidsperiode ikke ville forventes nogle tilfælde. Det svarer til en frekvens på ca. 1/40.000 vaccinationer, og med en statistisk usikkerhed, der betyder, at den reelle frekvens af VITT med 95% sikkerhed, er inden for intervallet ca. 1/20.000 til ca. 1/110.000 [12].
Der er forskellige estimater på tværs af lande, men Sundhedsstyrelsen har tiltro til det dansk-norske registerstudie, bl.a. grundet den høje kvalitet af de nordiske sundhedsregistre og den lette adgang til lægehjælp for borgerne, hvilket sikrer høj sandsynlighed for, at bivirkninger bliver indberettet. For personer <70 år har EMA fundet sammenlignelige frekvenser (1/48.000-1/100.000) baseret på opgørelser af bivirkningsindberetninger fra UK og EU (se Faktaboks – Vaxzevria®) [13]. I de britiske opgørelser ses en kønsfordeling sv.t. 57% kvinder og 43% mænd [13]. I alle bivirkningsovervågningssystemer er der risiko for underrapportering, ligesom der skal tages højde for forsinket rapportering.
Der er pr. 17. maj 2021 kendskab til i alt 11 tilfælde af mulig VITT efter 2. dosis af Vaxzevria® i EU og Storbritannien [14, 15]. Det kan aktuelt ikke med sikkerhed vurderes, om risikoen for VITT efter 2. stik med Vaxzevria® er højere, sammenlignelig eller lavere end risikoen for VITT efter 1. stik med Vaxzevria®. Det skyldes, at mange lande har valgt at udskyde 2. stik med Vaxzevria® til op mod 12 uger. Grundlaget for at bekrive frekvensen af VITT er derfor aktuelt for begrænset til, at det med sikkerhed kan vurderes, om der er en forskel på risikoen for VITT ved hhv. 1. og 2. stik.
Der er pr. 12. maj 2021 rapporteret i alt 28 tilfælde af VITT efter COVID-19 Vaccine Janssen® i USA, 22 blandt kvinder og 6 blandt mænd (se Fakta-boks – COVID-19 Vaccine Janssen®) [5].
Flere mulige tilfælde er aktuelt under vurdering. Alle 28 tilfælde er set i personer, der blev vaccineret, før USA pauserede COVID-19 Vaccine Janssen® den. 13. april 2021. Der må således forventes flere indrapporteringer samt risiko for underrapportering. Selv i en situation med global udrulning af COVID-19 vacciner, hvor opmærksomheden på bivirkninger er skærpet, er der indikationer på mulig underrapportering, og på forskelle mellem forskellige landes overvågningssystemer. For anafylaksi efter COVID-19 vaccination er der fx set en ca. 4-7 gange lavere estimeret frekvens i USA sammenlignet med Danmark baseret på bivirkningsindberetninger [16, 17].
COVID-19 Vaccine Janssen® er ikke taget i brug i Danmark, og først for nylig er vaccinen taget i brug i andre EU-lande. Der findes derfor aktuelt ingen europæiske eller danske data for frekvensen af VITT efter vaccination med COVID-19 Vaccine Janssen®.
Sundhedsstyrelsen finder, at det ikke med sikkerhed kan konkluderes, om den underliggende risiko for VITT efter COVID-19 Vaccine Janssen® er højere, sammenlignelig eller lavere end risikoen i forbindelse med Vaxzevria® [4]. For yngre kvinder er det dog rimeligt at antage, at risikoen er sammenlignelig mellem COVID-19 Vaccine Janssen® og Vaxzevria®. Det kan samtidig konkluderes, at mænd også kan udvikle VITT efter COVID-19 Vaccine Janssen®, men de begrænsede amerikanske data vanskeliggør vurderingen af, om VITT-risikoen hos mænd ved COVID-19 Vaccine Janssen® er højere, sammenlignelig eller lavere end hos kvinder.
Grundet mulig underrapportering i data fra USA har Sundhedsstyrelsen størst tiltro til risikoestimatet i det dansk-norske registerstudie, og at dette estimat er det bedste grundlag i en dansk kontekst for vurdering af risiko for VITT efter COVID-19 Vaccine Janssen®, dog med forbehold for større usikkerhed for estimatet hos mænd. Både EMA, Storbritannien og USA offentliggør løbende opdateringer af bivirkningsindberetningerne.
Sygdomsmekanismer og risikofaktorer for VITT
VITT er set udviklet fra dag 3 efter vaccination, typisk dog i uge 2 efter vaccination, og hos enkelte er det set op til 30 dage efter. Mekanismen menes at være relateret til auto-immun udvikling af anti-PF4 antistoffer. PF-4 ses på blodpladernes overflade. Anti-PF4 antistoffer kan udløse et fald i antallet af blodplader, dannelse af tromboser og risiko for blødning. Den præcise sygdomsmekanisme er endnu ikke fuldt afdækket [18].
Sundhedsstyrelsen kan ikke angive konkrete anbefalinger for målgrupper, herunder alder og/eller køn, der er uden risiko i forhold til at udvikle VITT efter COVID-19 Vaccine Janssen® eller Vaxzevria®. Forudgående kendt risiko for trombose eller trombofili, fedme, hormonbehandling mv. er heller ikke identificeret som risikofaktorer for VITT. Øget risiko for VITT kan måske skyldes endnu uafklarede faktorer som fx specifik vævstype eller tidligere autoimmunisering mv.
Det medfører, at lægen forud for vaccination med COVID-19 Vaccine Janssen® eller Vaxzevria® specifikt skal vurdere og informere den pågældende om den forventede forebyggelsesgevinst ved fremskyndet vaccination under tilvalgsordningen vejet op imod risikoen for VITT.
Håndtering ved mistanke om VITT
VITT er associeret med høj morbiditet og mortalitet og tidlig erkendelse, diagnostik og behandling er afgørende for behandlingssucces.
Patienter, der er vaccineret med COVID-19 Vaccine Janssen® eller Vaxzevria® bør varsles om tegn på VITT, herunder vedvarende hovedpine, intense, vedvarende mavesmerter, blødning i hud, symptomer på blodpropper, eller en kombination af disse, og instrueres i omgående at kontakte læge, hvis sådanne symptomer opstår 3-30 dage efter vaccination.
Vurdering af symptomer som mulig bivirkning til COVID-19 Vaccine Janssen® eller Vaxzevria® kan gøres i almen praksis og hos vagtlæge. Ved sammenhæng mellem symptomer på VITT og vaccination indenfor 3-30 dage bør patienten vurderes akut på sygehus. Hvis der efter vurdering på sygehus er klinisk og biokemisk mistanke om VITT bør den regionale koagulationsrådgivning kontaktes. Sundhedsstyrelsen har udarbejdet anbefalinger vedrørende diagnostik og behandling af patienter med mistænkt VITT efter COVID-19 vaccine, hvor den kliniske håndtering af patienter med mistænkt VITT uddybes [19].
Faktaboks - Symptomer på VITT
Patienter, der vaccineres med en af vaccinerne under tilvalgsordningen, skal informeres om at straks at søge læge, hvis de inden for 3-30 dage efter vaccination oplever ét eller flere af følgende symptomer:
- Intens vedvarende hovedpine
- Intense, vedvarende mavesmerter
- Blødning i hud/slimhinder
- Kliniske tegn på tromboemboli
eller kombination af ovenstående symptomer
Vedrørende brug af COVID-19 Vaccine Janssen® og Vaxzevria®
Vaccination med COVID-19 Vaccine Janssen® og Vaxzevria® anbefales ikke generelt af Sundhedsstyrelsen, da fordelene ved vaccination i den konkrete situation i Danmark ikke opvejer mulige skadevirkninger i form af VITT hos de vaccinerede, som fortrinsvis er yngre personer uden øget risiko for alvorligt forløb af COVID-19. Vurderingen er baseret på den aktuelle kontekst i Danmark, herunder smittetryk, sygdomsbyrde og epidemikontrol, samt andre tilgængelige vacciner.
Grundlaget for tilvalgsordningen for vacciner, der ikke generelt anbefales af Sundhedsstyrelsen, er beskrevet i bekendtgørelse med tilhørende vejledning, der beskriver særlige krav til det informerede samtykke, lægens ordination, delegation, journalføring mv. [20, 21].
Forud for vaccination med COVID-19 Vaccine Janssen® og Vaxzevria® under tilvalgsordningen er der skærpede krav til det informerede samtykke. Lægen skal specifikt vurdere og informere den pågældende om den forventet beskedne forebyggelses-gevinst ved fremskyndet vaccination under tilvalgsordningen og skal fremhæve, at vaccinen ikke generelt anbefales af Sundhedsstyrelsen, da fordelene ved vaccination i den konkrete situation i Danmark ikke opvejer ulemperne, og den pågældende i det generelle vaccinationsprogram gratis kan modtage en af de anbefalede vacciner. Lægen skal samtidigt specifikt nævne sjældne alvorlige komplikationer og bivirkninger ved vaccinerne (dvs. aktuelt VITT) samt nævne at der ikke kan angives køn eller aldersgrupper, der er uden risiko herfor.
Lægen skal endvidere informere om forholdsregler ved symptomer på de alvorlige bivirkninger iht. Sundhedsstyrelsens gældende anbefalinger vedr. diagnostik og behandling af patienter med mistænkt VITT efter COVID-19 vaccine [21].
COVID-19 Vaccine Janssen® og Vaxzevria® er kun godkendt til personer fra 18 år og ældre, og vaccination under tilvalgsordningen må alene ordineres til personer inden for vaccinens godkendte anvendelsesområde [20].
Habilitetserklæringer og referencer
kan ses på www.irf.dk
Referencer
- Organisering af vaccinations-indsatsen mod COVID-19 –
udrulning. https://www.sst.dk/-/media/Udgivelser/2021/Corona/Vaccination/Organisering-af-vaccinationsindsatsen-mod-COVID-19---udrulning_5_-februar-2021.ashx?la=da&hash=EEF79505F6ED87314714A2994B5A927774CB8FA9 - Vaccinationskalender. https://www.sst.dk/da/Udgivelser/2021/Vaccinationskalender
- EMA nyhed 7. april 2021. https://www.ema.europa.eu/en/news/astrazenecas-covid-19Vaccine-ema-finds-possible-link-very-rare-cases-unusual-blood-clots-low-blood
- EMA nyhed 20. april 2021. https://www.ema.europa.eu/en/news/covid-19Vaccine-janssen-ema-finds-possible-link-very-rare-cases-unusual-blood-clots-low-blood
- CDC. Advisory Committee on Immunization Practices (ACIP) mødemateriale 12. maj 2021. https://www.cdc.gov/vaccines/acip/meetings/slides-2021-05-12.html
- Greinacher A et al. Thrombotic Thrombocytopenia after ChAdOx1 nCoV-19 Vaccination. NEJM 9. april 2021. https://www.nejm.org/doi/full/10.1056/NEJMoa2104840
- Schultz NH et al. Thrombosis and Thrombocytopenia after ChAdOx1 nCoV-2 Vaccination. NEJM 9. april 2021. https://www.nejm.org/doi/full/10.1056/NEJMoa2104882
- Sundhedsstyrelsen. Fortsat udrulning af COVID-19 vaccine i Danmark uden Vaxzevria®. https://www.sst.dk/da/Udgivelser/2021/Vedroerende-fortsat-udrulning-af-COVID-19Vaccine-i Danmark-uden-Vaxzevria
- Sundhedsstyrelsen. Den danske COVID-19 vaccineudrulning fortsætter uden Johnson & Johnsons COVID-19Vaccine.https://www.sst.dk/da/Nyheder/2021/Den-danske-COVID-19Vaccineudrulning-fortsaetter-uden-Johnson-Johnsons-COVID-19Vaccine
- Produktresume Vaxzevria®, tilgået 10. maj 2021. https://www.ema.europa.eu/en/documents/product-information/Vaxzevria-previously-covid-19Vaccine-astrazeneca-epar-product-information_da.pdf
- Produktresume COVID-19 Vaccine Janssen®, tilgået 10. maj 2021. https://www.ema.europa.eu/en/documents/product-information/covid-19Vaccine--janssen-epar-product-information_da.pdf
- Pottegård A et al. Arterial events, venous thromboembolism, thrombocytopenia, and bleeding after vaccination with Oxford-AstraZeneca ChAdOx1-S in Denmark and Norway: population based cohort study. BMJ 5. maj 2021;373:n1114. https://www.bmj.com/content/373/bmj.n1114
- EMA Vaxzevria® visual risk contextualization. https://www.ema.europa.eu/en/-documents/chmp-annex/annex-Vaxzevria-art53-visual-risk-contextualisation_en.pdf
- MHRA Coronavirus vaccine – weekly summary of Yellow Card reporting. 13. maj 2021. https://www.gov.uk/government/-publications/coronavirus--covid-19Vaccine-adverse-reactions/coronavirusVaccine-summary-of--yellow-card-reporting
- EMA Vaxzevria article 5.3 -procedure assessment report 23. April 2021. https://www.ema.europa.eu/en/documents/referral/use-Vaxzevria-prevent-covid-19-article-53-procedure-assessment-report_en.pdf
- Lægemiddelstyrelsen. Status på behandlede indberetninger om formodede bivirkninger ved Comirnaty (Pfizer/BioNtech). 22. april 2021. https://laege-middelstyrelsen.dk/da/-nyheder/2021/status-paa-behandlede-indberetninger-om-formodede--bivirkninger-ved-comirnaty-pfizer-biontech/
- Lægemiddelstyrelsen. Status på behandlede indberetninger om formodede bivirkninger ved COVID-19 Vaccine Moderna. 22. april 2021. https://laege-middelstyrelsen.dk/da/-nyheder/2021/status-paa--behandlede-indberetninger-om-formodede-bivirkninger-ved-covid-19Vaccine-moderna/
- Greinacher A et al. Towards understanding ChAdOx1 nCov-19 vaccine-induced immune thrombotic thrombo-cytopenia (VITT. Preprint. 20 april 2021. https://www.researchsquare.com/article/rs-440461/v1
- Sundhedsstyrelsen. Anbefalinger vedr. diagnostik og -behandling af patienter med -mistænkt VITT efter COVID-19 Vaccine. https://www.sst.dk/-/media/Udgivelser/2021/Corona/Vaccination/Anbefalinger-vedrrende-diagnostik-og--behandling-af-patienter-med-mistnkt-VITT-efter-COVID19-Vaccine ashx?la=da&hash=1C6F0F9382-DECACD98362BCCBFEE-4E7BE801B5A0
- Bekendtgørelse om gratis vaccination mod COVID-19, BEK nr 928 af 19/05/2021. https://www.retsinformation.dk/eli/lta/2021/928
- Vejledning om vaccination mod COVID-19, VEJ nr 9352 af 19/05/2021. https://www.retsinformation.dk/eli/retsinfo/2021/9352